 |
| |
|
| |
醫療器材重要法規 |
| |
|
| |
第四條(藥物之定義)
本法所稱藥物,係指藥品及醫療器材。
第十三條(醫療器材之定義)
本法所稱醫療器材,係包括診斷、治療、減輕或直接預防人類疾病,或足以影響人類身體結構及機能之儀器、器械、用具及其附件、配件、零件。前項醫療器材,中央衛生主管機關應視實際需要,就其範圍、種類、管理及其他應管理事項,訂定醫療器材管理辦法規範之。
第四十條(製造與輸入醫療器材之文件與核可)
製造、輸入醫療器材,應向中央衛生主管機關申請查驗登記並繳納費用,經核准發給醫療器材許可證後,始得製造或輸入。...
|
| |
|
| |
|
| |
醫療器材GMP&QMS文件系統認證過程 |
| |
|
| |
 |
| |
|
| |
|
| |
|
| |
醫療器材分類分級 |
| |
|
| |
將醫療器材重新分為十七大類,共1750項,且依產品所具危險性高低,分為一(低危險性)、二(中危險性)、(高危險性)共三等級,管理模式如下: |
| |
一等級
(Class I)
|
二等級
(Class II)
|
三等級
(Class III)
|
| 低風險 |
中風險 |
高風險 |
|
約741項
(其中612項不須GMP&QMS)
|
約881項
均須GMP&QMS
|
約128項
均須GMP&QMS
|
須查驗登記
(簡化)
|
須查驗登記 |
須查驗登記 |
|
| |
|
| |
|
| |
GMP&QMS查核機構 |
| |
|
| |
1977年衛生署組成「醫療器材GMP&QMS推動小組」,完成GMP&QMS規範、實施細則等規定,已於87年8月10日與經濟部合銜公告,88年2月10日起實施
※醫療器材GMP&QMS代施查核機構
財團法人金屬工業研究發展中心
財團法人台灣電子檢驗中心
財團法人工業技術研究院量測技術發展中心
財團法人塑膠工業技術發展中心
|
| |
|
| |
|
| |
醫療器材優良製造規範的法規 |
| |
|
| |
依據藥事法相關規定、中國國家標準CNS
12681(ISO9001)及醫療器材品質保證制度國際標準(ISO 13485)訂定之,目前列入「藥物製造工廠設廠標準 第四篇」,共計二十一章。
|
| |

|
| |
|
| |
|
| |
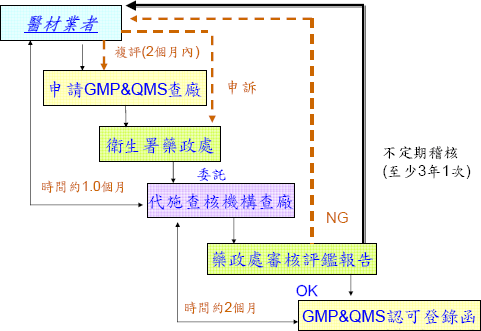
GMP&QMS申請模式 |
| |
|
| |
 |
| |
|
| |
|
| |
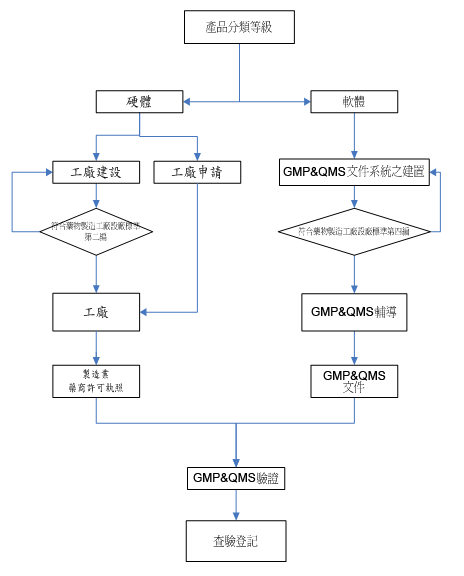
醫療器材GMP&QMS(暨查驗登記)認證過程 |
| |
|
| |
 |
| |
|

|
| |

